がんの基礎知識Our Service
がん遺伝子治療|ジーテック
人間の体は、約60兆個の細胞から成り立っています。細胞は増殖と自滅を繰り返しながら、60兆個というバランスを上手く維持しています。逆に、がんは、「がん遺伝子」の暴走と、その暴走をとめるはずの「がん抑制遺伝子」の機能不全によって、異常細胞の「無限増殖」と「不死」が起こっている状態です。
元々は正常だった遺伝子(がん原遺伝子)が、様々な要因によって傷つき、機能や構造が変異して、細胞増殖のアクセルが踏まれたままの状態になることがあります。このような遺伝子が、がん遺伝子で、正常細胞のがん化を引き起こします。これまでに200以上の遺伝子ががん原遺伝子として同定されています。がん原遺伝子はタンパク質の構造変化、活性化、増大によって、細胞分裂の引き金を引くことになります。
多くの場合、がん遺伝子によってつくられるタンパク質は、その働きが異常に強くなることにより、細胞増殖のアクセルが踏まれたままの状態になります。
例えば、「myc」と呼ばれるがん遺伝子の場合、1個の細胞あたりの遺伝子の数が増えることにより、「myc遺伝子」によりつくられるタンパク質が増えすぎて、際限ない細胞増殖を引き起こすことがわかっています。
-

-
がん抑制遺伝子
がん遺伝子を車に例えると、がん遺伝子が車のアクセルです。そして、ブレーキにあたる遺伝子が、がん抑制遺伝子になります。がん抑制遺伝子の働きには、細胞の増殖を抑制、細胞のDNAに生じた傷を修復、細胞にアポトーシス(細胞死)を誘導したりするなどがあります。DNAの傷が蓄積されると「がん化」に結び付きますので修復が必要になります。また、異常を感知して、異常細胞が無限に増殖しないように、その細胞に細胞死を誘導することも必要です。これらのことを考慮すると、がん抑制遺伝子がブレーキの働きをしていると考えられます。
①増殖を抑制するPTENという「がん抑制遺伝子」
②自滅を促進するp53という「がん抑制遺伝子」
③老化した細胞を排除するp16という「がん抑制遺伝子」
60兆個の細胞がバランスよく維持されているのは、これらの作用によります。
がんの状態は、「無限増殖」「不死」です。
→ですから、がん遺伝治療は、遺伝子異常のあるがんの原因を改善することです。
Ⓐがんの場合、ほとんどのがん組織で、がん抑制遺伝子の機能が低下が見られる
→そのため、がんの原因となっている「がん抑制遺伝子」を投与するのが、がん遺伝子治療です。
「がん抑制遺伝子」には、p53・p16・PTEN・(GATA3)などがあります。
Ⓑがんには、増えるとよくない蛋白があります。
蛋白には、下記のようなものがあります。
・がんの増殖を促進させる:CDC6
・がんの発現に関係する:EZH2
・がん抑制機能を阻害する:ガンキリンなど
これらの蛋白を作るには、蛋白を作るためにマイクロRNA(mRNA)が増加します。
→ですから、このmRNAを抑制するRNAを投与するのが、がん遺伝子治療になります。
投与するRNAの例)EZH2抑制RNA・CDC6抑制RNA・ガンキリン抑制RNA
-
-
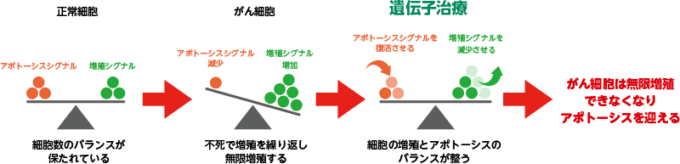
がん遺伝子治療
遺伝子の異常や欠如が「がんの発生」に、大きく関係していると言われています。がん細胞を調べると、実際にがん抑制遺伝子がほとんど正常に機能していなことがわかりまます。そのため、がんの代表的な特徴である「無限増殖」と「不死」という現象が起こるのです。ですから、がんの無限増殖を抑制するには、このような遺伝子の異常によりがん化した細胞に、遺伝子を正常に導く治療タンパクを投与することです。この逆の働きでアポトーシス(がん細胞の自滅)を促進させることが出来ます。このようにがんの原因である遺伝子異常を改善するのが、がん先端治療であるがん遺伝子治療です。
がん抑制遺伝子が働かない → がん細胞が無限増殖する → がん抑制遺伝子を投与 - もう一つは、先ほどがん遺伝子のところで、タンパクが増えると良くないとご紹介しました。このタンパクを作るマイクロRNA(mRNA)という物質が増加する場合は、mRNAを抑制するRNAを投与します。
がん遺伝子治療の効果を左右する2つのポイントがあります。
①どのような多種の治療タンパク(抑制遺伝子やmRNA)を使うか
②がんに対して高濃度の治療タンパクを届ける優れたベクターを使うか
*ベクター:「運び屋」と考えてください
常にがん遺伝子治療も進化しており、
・さまざまながん抑制遺伝子やマイクロRNAなど治療タンパクの開発状況
・対応している治療タンパクの多様性
・がん組織になるべく高濃度の治療タンパクを効率的、効果的に届けられるベクター、デリバリーシステムの開発状況
を確認しながら、開発、対応状況が進んでいる医療機関をご案内できるよう心がけています。
-
-
遺伝子治療は、がんの種類や病期を問わず優れた効果を発揮します。がんは遺伝子の異常から発現するため、原因となっている遺伝子に直接作用する遺伝子治療がほとんどのがんに効果を示すのは当然のこととも言えます。
- 自滅促進型と増殖抑制型(分子標的薬)という抗がん剤があります。
・p53というがん抑制遺伝子は、自滅を促進します。
・p16というがん抑制遺伝子は、老化した細胞を排除するDNAに対する働き方が、自滅促進型の抗がん剤と似ているので、相乗効果を示します。
・損傷のある細胞を攻撃する放射線治療は、p53、p16は同じく損傷のある細胞を自滅に追い込むという点で、放射線治療とも相乗効果を示します。
また、増殖を抑制するPTENというがん抑制遺伝子は、増殖抑制型の抗がん剤と同じように増殖シグナル抑制に対して働くため、やはり相乗効果を示します。
このように、がん遺伝子治療は、抗がん剤や放射線治療と働き方が似ているため、相乗効果が高く、標準治療との複合治療は、より大きな効果が期待されます。しかも、主に点滴投与による治療であり、苦痛のない、副作用もほとんどない、肉体的にも、精神的にも優しい有効な治療です。
-
-
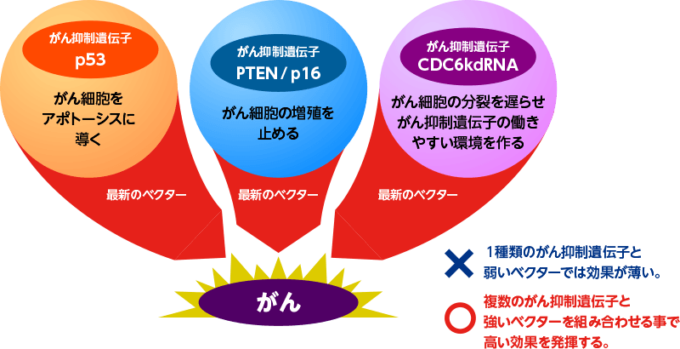
治療タンパクとベクター
がんの究極的な難題は、細胞の「不死」と「無限増殖」です。したがって、「無限増殖」であるがん細胞の増殖を止める、「不死」であるがん細胞をアポトーシス(自滅)に導く、この2つの方向からがん細胞を攻撃することが必要であり重要です。この2つは同じように感じますが、実は違う遺伝子が異なる作用の仕方で働いています。従来の遺伝子治療では、どちらか一方の効果しか認められない遺伝子のみを提供する医療機関もありました。しかし、がんの「不死」と「無限増殖」に対し、それぞれに効果の高い治療タンパクを使用するのが最新のがん遺伝子治療です。また、患者さんの遺伝子の特徴が、がん遺伝子検査によって把握できれば、より精度の高い遺伝子の選別と投与を可能とします。
- p53、p16の働きは「不死」に対して示されます。
PTEN、CDC6抑制RNAは、「増殖」に対して働きます。
EZH2抑制RNAは、がんの「発現」という特徴に関係するEZH2というタンパク質を抑制します。
そして、ガンキリン抑制RNAは、がんに対して「がん抑制遺伝子の阻害」を抑制する働きがあります。
がんの特徴である「不死」「増殖」「発現」「阻害」という特徴に、それぞれに働く治療タンパクを複数、組み合わせて使用することが重要です。
これらの治療タンパクを投与には、がん組織に高率に到達させるためにベクターが欠かせません。ベクターは、運び屋の役割をしています。その役割は、治療タンパクを体内のがん細胞に届けることです。がん細胞にまで安全に安定して届けるために、どんな種類のベクターを使うかが非常に大切になります。
当初の遺伝子治療では、アデノウイルスというベクターを用いていましたが、発現期間が短く、細胞の核に入り込む可能性も少ないため遺伝子治療のベクターとしては不十分なものでした。遺伝子治療の効果は大きく前進させたのは、後に発現期間が長く、細胞の核にまで容易に入り込むレンチウイルスを使用することです。
り改良した特殊なベクターが最新の遺伝子治療で使用されています。
①正常な血管には通過しないで、粗造ながんの血管壁だけが通過する大きさ(100nm前後)に揃えるために、ベクターを最新の高分子ミセル化します。(ドラックデリバリーシステム=DDS)
②ヒトテロメラーゼという酵素が働いているので、がんや幹細胞が無限に増殖されいます。半特異的にがん細胞の中で反応させるために、このヒトテロメラーゼに反応するヒトテロメラーゼ逆転写酵素を付けます。
③がん細胞の核内へがん抑制遺伝子を侵入させ長期発現させることが特殊なベクターにより可能です。
がん抑制遺伝子や抑制mRNAが進化を続け、より効果的なベクターによってがん細胞に到達します。
「p53」
「ゲノムの守護神」とも言われているp53の働きによって、人が生まれてから死ぬまでの期間、つま先から頭の先までのすべての細胞である30億の遺伝子情報が維持されています。がん抑制遺伝子であるp53は、細胞分裂の時のDNA修復を指示する、DNA損傷が強い場合は細胞死(アポトーシス)を指示するなど、DNAに傷を持っている細胞を制御する機能を持っており、がん化した細胞にアポトーシスさせます。がん抑制遺伝子は、がんと最も深い関わりのあるとも言われていて、約60%のがん患者さんには(再発の患者さまの場合は、ほとんどの方に)がん組織内にp53遺伝子の変異・欠損・機能障害が認められます。
がんはp53が働けないように、p53と結合するMDM2というタンパクを多く産生したり、p53に対する抗体を作る場合もあり、p53の働きを抑制するために策を講じています。そのため、単純にp53をがん組織に投与してもなかなか本来の働きをしてくれません。
最新の遺伝子治療で使用されるp53は、MDM2やp53抗体になるべく反応しないように改良されているので、優れた治療効果が見られるようになりました。
一般的にp53遺伝子に変異を持つがんでは、抗がん剤や放射線などの治療に抵抗性が存在します。がん細胞のDNAに傷をつけるような抗がん剤治療や放射線治療に対し、p53による、がん細胞のアポトーシスへの誘導効果を合わることで、抗がん剤治療や放射線治療の効果の増強、相乗効果を示します。
「PTEN」
p53に並ぶ代表的ながん抑制遺伝子と考えられているPTENは、約50%のがん患者さんに(再発の患者さんはほとんど)がん組織内に機能障害が認められます。通常、細胞の増殖シグナルを脱リン酸化という作用で遮断したり、細胞増殖を停止させるのがPTENです。特にがんの激しい増殖に最も関与している「がん抑制遺伝子」と言えるのは、PTENが働けないことからわかります。
がん細胞の増殖が加速されるのは、がん組織においてPTENの働きが阻害されてしまうと、がんの増殖シグナルを遮断できず、がん組織において血管新生が促進されるので増殖因子が多く作らることによります。PTENを投与することによって、細胞の増殖シグナル経路の途中の伝達物質を脱リン酸化させるので増殖シグナルを遮断させ、過剰な増殖をするがん細胞を阻害します。PTENによって増殖阻害された細胞は、やがて細胞死します。
がん細胞の増殖シグナルを遮断するPTENは、増殖を抑制しますからPTENと同じ経路で働く抗がん剤(増殖抑制型抗がん剤=分子標的薬やホルモン剤)と相乗効果が示されます。
「p16」
細胞老化に関係するがん抑制遺伝子であるp16は、細胞の異常な増殖を防ぎ、がんの発生を予防してくれるものなので、正常な細胞ではほとんど機能していません。しかし、細胞分裂周期中に細胞分裂を遅らせたり、異常細胞を排除を老化して要らなくなった細胞が行なっています。
p16は、約30%の患者さんには(再発の患者さんはほとんど)がん組織内に機能障害が認められるがん抑制遺伝子で、特に高い確率で欠損が見られるのは、喫煙者の肺がんなどです。
p16が投与されることで、がんの新生血管形成が阻害、細胞分裂において一番重要な分裂期への移行のストッパーとしての働きをします。また、p16は他のがん抑制遺伝子が正常に機能できる体内環境を作る役割も持っています。
がん細胞の増殖を抑制して自滅排除するp16の投与は、抗がん剤との併用で相乗効果を示します。
「CDC6抑制RNA」
CDC6は、細胞を増殖させるために働くタンパク質ですから細胞の周期を調整する働きを持っています。通常、細胞周期の初期の段階で少量のみ現れるのですが、ほとんどのがん細胞では周期に関わらず大量にCDC6が発現してしまうので、がん細胞の増殖の元となる細胞分裂を増進することになります。また、がん細胞を無限増殖させるアクセル役だけでなく、細胞増殖を抑制するがん抑制遺伝子の働きをも抑制するので、ブレーキも効かなくしてしまいます。
CDC6を作る部分ではmRNAがコピーの役割を行い、がん細胞においてもmRNAがCDC6の製造増加に関与しているので、逆にCDC6の生産を抑制させるmRNAを投与して、これに反応させて(RNA干渉)させ、CDC6生産を抑制します。
このようにmRNAに反応させて、生産されるタンパクを抑制させる方法をRNA干渉といいます。このRNA干渉を発見した功績により、2006年にはスタンフォード大学教授アンドリュー・ファイアーとマサチューセッツ工科大学教授クレイグ・メローが、ノーベル生理学医学賞を受賞しています。
がん細胞は大量にCDC6を産生するので、RNA干渉を利用してCDC6の産生を抑制します。
またCDC6の抑制はp53などのがん抑制遺伝子が働きやすい環境を作ります。
「ガンキリン抑制RNA」
ガンキリン抑制RNAの働きは、ガンキリンの産生を抑制させるために、がん抑制遺伝子の働きを阻害させることです。このガンキリンは、厄介なタンパク質です。ガンキリンは、1998年にヒトの肝細胞がんから発見された新しいがん遺伝子(悪者)で、ほぼ全てのがんに含まれていることがわかっています。その機能が従来がんを抑制する、p53、p16、PTEN、RBなどのがん抑制遺伝子の働きを阻害してしまいます。
がん抑制因子を阻害するガンキリンは、「不死」「増殖」、がんの「発生」から「転移」「浸潤」というがん細胞の特性を至る所で阻害するので、標準治療の効果さえも低下してしまいます。
ほとんどのがん細胞で高頻度で高発現されるガンキリンの発現が多いほど、浸潤、転移が多くなり、予後不良であることが残念ならが認められています。
「ガンキリン抑制RNA」は、ガンキリンによって阻害されていたがん抑制遺伝子が本来の働きを取り戻して、がん細胞の消滅を効率的に促進するために、ガンキリンをつくるRNAに反応させて、RNA干渉を利用することで、ガンキリンの発現を抑えます。私たちの治療タンパクを作成しているアメリカで「ガンキリン抑制RNA」は、開発され作られました。
ガンキリンを抑制することが、より効果的に従来の遺伝子治療が行なえます。
「EZH2抑制RNA」
細胞を発現させるために働くタンパク質であるでEZH2は、がん細胞などの発現にも大きく関与しています。
EZH2が多量に存在する場合は、進行の早いがん組織に見られます。発現力が強く進行も速いEZH2が多く存在するがんは、予後の悪いがんです。
この発現に関与するEZH2も、CDC6同様に正常な遺伝情報からmRNAのコピーで作られます。そこでEZH2を作るmRNAに働く、EZH2抑制RNAを投与し、やはりRNA干渉を利用してEZH2の産生を抑制します。
EZH2を抑制させることは進行の早いがんや再発予防に重要な働きをします。
現在EZH2を抑制させる抗がん剤を研究開発中です。
「その他のがんを抑制する因子の開発」
遺伝子治療は日々、進化しています。最新のがんを抑制する因子の開発を私たちも提案しています。
今後加わる予定のものとして、現在開発中の乳がんの、特にトリプルネガティブに関係すGATA3/GATA4というがん遺伝子に働きかける遺伝子治療などがあります。
乳がん全体の15%程度をトリプルネガティブ乳がんが占めており、女性ホルモンによって増殖する性質を持たないため、これに対応するホルモン療法では有効でなく、また、がん細胞の増殖にかかわるタンパクのHER2も陰性であるため、この分子標的薬も効かず、抗がん剤による治療しかなく、あまり予後についても良くないと言われています。
細胞増殖過多を抑える考え方のがん遺伝子治療は、がん遺伝子からの産物によります。現在は、がん遺伝子治療や抗がん剤においても、がん抑制遺伝子からのアプローチがほとんどです。私たちは、もう一つの原因であるがん遺伝子から出る物質による細胞増殖の抑制も考えています。
「最新のベクター」
ウイルス性を持たないベクターを開発したのは、開発に次ぐ開発を2001年から行なっていた、遺伝子治療薬研究の第一人者であるアメリカのローフェン博士です。最新の研究によって、レンチウイルスの病原性を完全に排除し、運び屋としての役割のみを追求して作り上げたものです。さらに、高分子ミセル化(優秀なドラッグデリバリーシステム)され、従来のベクターよりがん細胞にさらに核内に侵入しやすくなり、治療タンパクの効果を高めることができました。
さらに、藤田潤先生との共同作業により、ガンキリン抑制RNAも登場しました。
これにより近い将来、がん遺伝子治療の経口薬を開発できる可能性も高まりました。
また現在は、大きさを100nm前後の高分子ミセル化して、病原性を完全に排除し、核内にまで入り込む発現期間が長いものが使用されています。
-
-
最新の遺伝子治療
「有効多種の治療タンパク」
「無限増殖」「不死」をはじめとするさまざまな特徴(発現や抑制遺伝子への阻害など)があるがんには、単一のがん抑制遺伝子、治療タンパクでは効果が限られており、状況にあったバラエティーな障害のすべてに対応できているとは限りません。
CTC検査(末梢循環腫瘍細胞、Circulating Tumor Cell)を実際に患者さんに受けてもらい、がんを調べてみると、浸潤、転移、血管新生、増殖シグナル、受容体、細胞周期、不死など、多種にわたり障害を見られます。 - したがって治療は、複数のがん抑制遺伝子やmRNAを用いて、がん細胞の増殖を抑える、アポトーシスに導くなどいろいろなアプローチする必要があります。
また、がん抑制遺伝子ががん細胞まで運ぶベクターの働きも重要です。がん抑制遺伝子が十分に働くことができないベンターは、細胞の核内にまで入り込めないベクターや発現期間の短いベクターです。運び屋のベンターの大きさも重要で、しっかとしたドラッグデリバリーシステム(DDS)を持つことが大切です。また、EPR効果(腫瘍に対して高濃度でより多く、そして長く保持させる効果)を上げる努力も重要です。
がん抑制遺伝子に非常な重要なp53ですが、多くのがん組織内ではp53の働きを抑制として働くp53抗体や多量のMDM2が存在するので、そのままのp53では、阻害されてしまいp53の十分な効果が得られません。さらに、抗がん剤や放射線治療の効果によってもp53の機能低下してしまいます。
標準治療やがん遺伝子治療の重要な鍵となるのは、MDM2やp53抗体に反応しにくいp53を用いることです。
さらに、主要ながん抑制遺伝子(p53などの)がより働きやすい環境とするために、ガンキリン抑制RNAを追加することは、十分にがん抑制遺伝子の機能が発揮されます。
「がん細胞に有効に到達させる努力」
私たちが注目しているがん遺伝子治療は、遺伝子治療薬研究の第一人者であるアメリカのローフェン博士が開発した最新のがん遺伝子治療で、現在も日々発展を続けています。使用する治療タンパクは現在5種類ですが、今後も増加する見込みです。ベクターも高分子ミセル化しているので、大きさを80nm~100nm前後にして、病原性を完全に排除し、核内にまで入り込む発現期間が長いものを使用しています。
このようにがん細胞に有効に到達させるため、最新の遺伝子治療では様々な努力によって進化し続けています。
私たちの推奨したいがん遺伝子治療では、治療タンパクが腎臓から排泄されにくく、約3~5日で体を循環することでがん組織を探します。
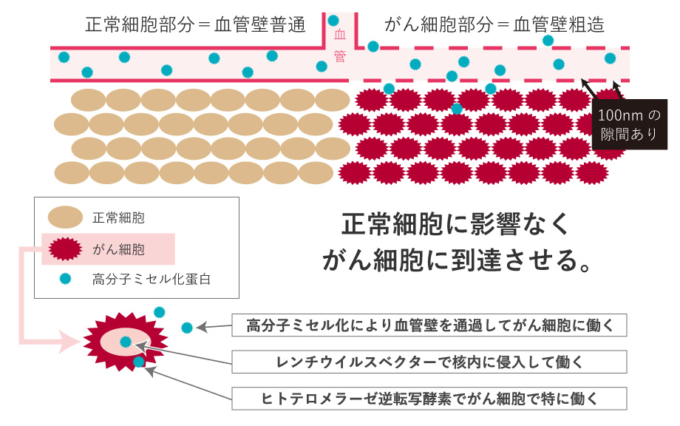
①高分子ミセル化
正常な血管は通過せず、がんが作る粗造な血管壁だけを通過する大きさ(80nm~100nm前後)に整えて、がん到達率を高めます(ドラックデリバリーシステム=DDS)。
高分子ミセル化とは、この大きさにすることで、抗がん剤もこの大きさに変える研究が現在行われています。
これにより高率よくがんに入り、副作用が少ない抗がん剤ができます。
②ヒトテロメラーゼ逆転写酵素(h-TERT)を利用
細胞分裂の時DNAの転写はテロメアという部分から始められます。分裂するたびに削られてゆくテロメアは、無くなったら細胞は死を迎えます。そのため、テロメアは「細胞の死の回数券」ともいわれます。
しかし、無限にテロメアを作るヒトテロメラーゼという酵素をがん細胞や幹細胞は、持っています。このヒトテロメラーゼによりがんや幹細胞は無限にテロメアを作り続けることができるので、無限に分裂します。
がん細胞の中で大きく反応させるのは、このヒトテロメラーゼの特徴を利用してヒトテロメラーゼ逆転写酵素(h-TERT)を付けることです。また、がん細胞に対して半特異的に反応させます。
③非ウイルス性(特徴はレンチウイルス)ベクター
病原性を完全に排除した上で、さらに安全性を高め、レンチウイルスが持つ、核内に長く留まるという性格のみを生かす、「非ウイルス性ベクター」の開発に成功しました。「非ウイルス性ベクター」の開発は、さらにがん抑制遺伝子を核内に高率的に運び込み、長期発現することができます。
つまり高分子ミセル化でがんに寄せ、h-TERTでがん細胞に半特異的に反応させるので、レンチウイルスの性格で核内にがん抑制遺伝子を届ける、ということです。
-

-
がん遺伝子治療の優れた特徴
1.副作用が少なく軽い
副作用として、発熱、頭痛、血圧変動が起こる場合がありますが、解熱剤やごく少量のステロイドを投与することで、副作用はほぼ抑えることが出来ます。アナフィラキシーショック(軽い反応のみ)の発生率は0.3%以下です。
2.正常細胞に影響を与えない
元々体の中にある、正常細胞に備わっている遺伝子ですから、投与しても正常細胞への影響はありません。 - 3.抗がん剤や放射線治療の効果を補強
抗がん剤や放射線治療は、細胞分裂の際にがん細胞のDNAを傷つけ、あるいはDNAデータがコピーされるのを阻止して、細胞を自滅させます。遺伝子治療もDNAに損傷のあるがん細胞を排除するという点では同様の作用ですので、効果を補強することができます。また、分子標的薬の増殖阻止と遺伝子治療PTENは、同じ経路で働くため、相乗効果を示します。抗がん剤に対して耐性が出来たがん細胞にも有効ですので、併用により効果を増します。
4.細胞レベルでがんに対処
遺伝子治療の効果は、血管やリンパ管から全身の細胞に広がりますので、見えないレベルの転移や、手術後の再発予防にも有効です。抗がん剤の代わりとしても有効に使用することができます。
5.前がん状態、がん予防にも有効
がん発症に至っていなくても、がん抑制遺伝子が正常に機能していない状態の細胞にも作用します。前がん状態にある細胞の増殖を止めたり、自滅に追い込むことができます。がん発症の予防にもなります。
6.耐性ができない
遺伝子治療では、直接がん細胞内に入り作用するので、耐性ができて効果が得られなくなるということがありません。したがって長期間にわたって使い続けることも可能です。
7.がん幹細胞や難治性のがん細胞にも有効
抗がん剤や放射線が効きにくい、がん幹細胞やストレスに強いがん細胞や、抗がん剤の作用にも打ち勝って生き残り増殖した難治性の再発がんにも、直接がん細胞内に入り込んで威力を発揮します。
8.治療適用範囲が広い
標準治療と併用することも可能ですし、相乗効果があります。副作用が少ないので、発がん予防、再発予防、再発がん対処、末期がんまで幅広く利用できます。仕事をしながらでも、体力の衰えた患者さんでも使用できます。
9.どのがんにも有効
がん細胞の異常遺伝子に直接作用するため、がんの種類や部位を問わず、有効です。抗がん剤の効きにくい、がん幹細胞やストレスに強いがん細胞、難治性のがんにも効果が期待できます。
10.場所を選ばない
点滴投与もしくは、がん腫瘍部分への直接注入になります。どちらも簡単なので、入院や特別な施設、機械などは必要がなく簡単な措置です。
-

-
副作用について
抗がん剤のような強い副作用は、がん先端治療である遺伝子治療にはありません。
アナフィラキシーショックやアレルギー反応やがごく稀(0.3%以下)に起こる可能性が治療タンパクを使うためにありますが、安全確認のために事前にアレルギー反応テストを行なった後に、治療が始まりますから、ほとんどが軽症です。
また、高分子ミセル化という技術を治療タンパクのがん到達率を高めるために用いています。高分子ミセル化に関する副作用には、微熱、頭が重い、頭痛といった症状の他に、体内の血流が増す現象が起こることが時々あります。これらの副作用の発生率は15%程度であり、症状が出た際には、軽い痛み止め(解熱鎮痛剤)を服用することですぐに症状は改善しています。
